Uranio

Uranio enriquecido.
See page for author [Public domain], via Wikimedia Commons
El uranio es el elemento natural más pesado. Es un metal de color plateado, duro y radioactivo que debe su nombre al planeta Urano.
Se origina de forma natural durante las explosiones de las supernovas. Con 92 protones, es el elemento de mayor peso atómico que se encuentra en la naturaleza, y su núcleo puede descomponerse, emitiendo partículas alfa (uniones de dos neutrones y dos protones). En contacto con el aire pierde su brillo y si está finamente dividido, estalla en llamas.
El brillante polvo negro que el químico Klaproth aisló de la pechblenda en 1789, solo ocho años después del descubrimiento de Urano, era en realidad un óxido de uranio. Cincuenta y dos años más tarde, Eugène Melchior Peligot obtuvo el elemento al reducir el tetracloruro de uranio con potasio.
El uranio y la radioactividad
Durante el siglo XIX, no era considerado peligroso y se utilizaba como pigmento para colorear cerámica y vidrio.
En 1896, Henri Becquerel descubrió que al colocar sales de uranio sobre una placa fotográfica, esta se ennegrecía a causa de la radiación emitida por las sales de uranio. Dicha radiación atravesaba papeles negros y sustancias opacas. Marie Curie, dedicó su tesis doctoral al estudio de esa radiación y sus efectos acuñando el término «radioactividad».
Cada vez que un elemento inestable como el uranio desprende una partícula se transforma en otro elemento. Este fenómeno se conoce con el nombre de decaimiento. El uranio decae pasando por el torio y el protoactinio hasta que se transforma en un estable núcleo de plomo.
El uranio natural está formado por tres tipos de isótopos: uranio-238 (99,284%), uranio-235 (0,711%) y uranio- 234 (0,0085%). La relación uranio-238/uranio-235 es constante en la corteza terrestre, salvo ciertas excepciones, como ocurre en los yacimientos de Oklo donde hay evidencias de que hace unos 2000 millones de años se produjeron reactores nucleares naturales.
La desintegración de los isótopos naturales del uranio genera calor que contribuye a mantener la temperatura interna de la Tierra y su campo magnético, ambas condiciones imprescindibles para mantener la vida en nuestro planeta.
Aplicaciones

Central nuclear.
Sturm [CC BY 3.0], via Wikimedia Commons
El uranio se emplea como combustible en los reactores nucleares, encargados de producir el 3% de la energía que genera el hombre a nivel mundial. Además, es utilizado en la elaboración de municiones perforadoras y planchas de alta resistencia.
El U-235 es el isótopo fisible, por eso es necesario aumentar la concentración de este isótopo en el uranio natural para poder utilizarlo como combustible y en la fabricación de bombas.
Otros usos y aplicaciones son:
• Edificación de estabilizadores para los aviones y satélites artificiales.
• Elaboración de cristales con una coloración verde y amarilla incandescente.
• El U-238 es convertido en plutonio y este a su vez puede ser empleado como arma nuclear.
• El U-238 es aprovechado como blindaje contra altísimas radiaciones.
• En estado metálico,es utilizado como blanco de rayos X y para la realización de los mismos.
• Como blindaje de los tanques de guerra y algunos misiles
• Algunos fertilizantes de fosfato poseen uranio.
Little Boy
El 6 de agosto de 1945 a las 8:16a.m. se lanzó sobre la ciudad japonesa de Hiroshima la primera bomba atómica de uranio. Los aliados habían realizado una prueba en el campo de tiro de Alamogordo con una bomba de plutonio.
Little Boy, el nombre en clave del artefacto, contenía la cantidad necesaria de U-235 (unos pocos kilogramos) para iniciar la reacción en cadena que liberara, en una fracción de segundo, una gran cantidad de energía.
El uranio enriquecido se obtuvo convirtiendo el metal en hexafluoruro de uranio, un compuesto volátil que sublima a 57 ºC. Como los dos isótopos se diferencia en su peso atómico sus compuestos se pueden separar por difusión.
El poder destructivo de la bomba fue equivalente al de 12500 toneladas de TNT. Destruyó casi 50000 edificios y más de 75000 personas murieron directamente o en un mes debido a las quemaduras.
Contenido relacionado
 Marie Curie
Marie Curie
Marie Curie (Varsovia, 1867 – 1934) fue pionera en el campo de la radiactividad. Tras años de trabajo […]
 El radio
El radio
El radio fue descubierto por Marie y Pierre Curie en 1898. El matrimonio halló el radio en una variedad […]
 Cosméticos radiactivos
El descubrimiento de radio en 1898 por Marie y Pierre Curie generó un gran interés científico. Este elemento tan sorprendente enseguida encontró aplicaciones comerciales que reflejaban las esperanzas puestas en esta sustancias y sus espectaculares propiedades.
Cosméticos radiactivos
El descubrimiento de radio en 1898 por Marie y Pierre Curie generó un gran interés científico. Este elemento tan sorprendente enseguida encontró aplicaciones comerciales que reflejaban las esperanzas puestas en esta sustancias y sus espectaculares propiedades.  Cuerpos celestes en la tabla periódica
¿Cuántos planetas y objetos celestes puedes encontrar en la tabla? Entre los 118 elementos químicos recogidos en la última versión de la tabla periódica podemos encontrar 10 elementos relacionados con cuerpos celestes, aunque también, puede ser que el nombre haga referencia al personaje mitológico con el que también se relaciona dicho planeta u objeto.
Cuerpos celestes en la tabla periódica
¿Cuántos planetas y objetos celestes puedes encontrar en la tabla? Entre los 118 elementos químicos recogidos en la última versión de la tabla periódica podemos encontrar 10 elementos relacionados con cuerpos celestes, aunque también, puede ser que el nombre haga referencia al personaje mitológico con el que también se relaciona dicho planeta u objeto.  ¿Por qué se producen las explosiones?
¿Por qué se producen las explosiones?
Una explosión es una combustión muy rápida en la que se libera un gran volumen de gases que […]



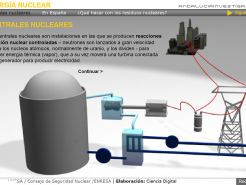 Energía nuclear
Energía nuclear 