La teoría atómica: Átomos y moléculas, elementos y compuestos

¿De qué está hecho el mundo que nos rodea? La teoría atómica es la teoría científica que afirma que la materia está compuesta de unidades discretas denominadas átomos, la cual ha ido cambiando a lo largo del tiempo al incorporar las nuevas evidencias experimentales.
Los griegos ya se planteaban que al dividir una sustancia llegaría un momento en el que se obtendrían partículas indivisibles a las que denominaron átomos. Leucipo, Demócrito y Lucrecio ya utilizaron este término basándose en argumentos filosóficos y no experimentales.
Entre 1803 y 1807, Dalton propone el primer modelo atómico que le va a permitir explicar las leyes experimentales que determinan las proporciones en las que reaccionan las sustancias para formar los compuestos (conservación de la masa, proporciones definidas y proporciones múltiples). Dalton afirma que la materia está compuesta por unas partículas indivisibles denominadas átomos que se combinan entre sí para formar compuestos en una relación de números enteros y sencillos, y que los átomos de un mismo elemento son iguales en masa y presentan las mismas propiedades.
El descubrimiento del electrón en los tubos de descarga de gases llevó a Thomson a enunciar que el átomo era divisible y que consistía en una masa cargada positivamente que contenía a los electrones. Este modelo tuvo que ser modificado para incluir las evidencias experimentales aportadas por Rutherford, Geiger y Marsden que que llevaron al primero a plantear el modelo planetario. El átomo estaría en su mayor parte vacío y los electrones girarían alrededor de un núcleo compacto cargado positivamente. El descubrimiento del protón y la determinación de su masa y carga llevó a postular la existencia en el núcleo de otra partícula, el neutrón, que permitiera explicar el déficit de la masa del núcleo si en este solo se encontraban protones.
Un elemento químico vendrá definido por el número de protones que contenga su núcleo; así pues, podremos tener átomos del mismo elemento con distinta masa y distintas propiedades en función del número de neutrones que contenga (isótopos).
Los átomos al unirse forman compuestos. La molécula es un grupo eléctricamente neutro y suficientemente estable de al menos dos átomos en una configuración definida, unidos por enlaces químicos fuertes.
El modelo de Rutherford nos permite explicar estos conceptos, pero será necesario introducir los principios de la física cuántica para elucidar el comportamiento de las partículas subatómicas.
Contenido relacionado
 ¿Qué es el número atómico?
¿Qué es el número atómico?
Atómico significa relativo al átomo, la porción más pequeña en que puede dividirse un elemento químico manteniendo sus […]
 ¿Qué es un elemento químico?
¿Qué es un elemento químico?
Un elemento químico es una sustancia pura (o especie química definida) cuyas propiedades intrínsecas lo diferencian de otros […]
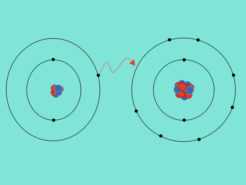 ¿Cómo se forman los enlaces químicos?
¿Cómo se forman los enlaces químicos?
Los enlaces químicos se forman ganando, cediendo o compartiendo electrones para alcanzar configuraciones electrónicas estables como por ejemplo […]



