¿En qué proporciones se unen unos elementos con otros?
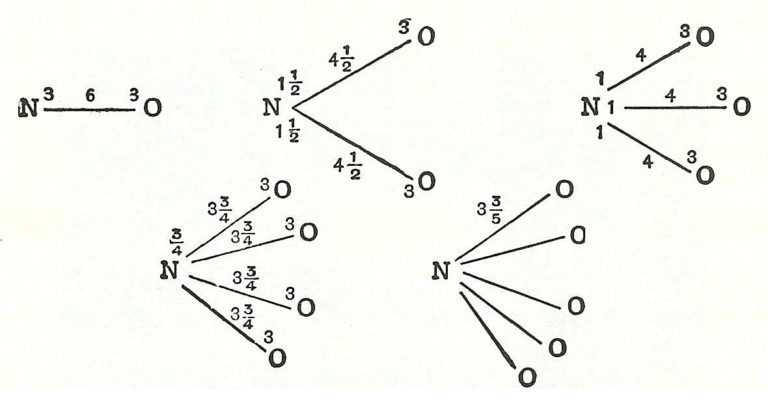
Los elementos químicos se unen en función de sus ‘valencias’ tomando como referencia el hidrógeno.
Esto quiere decir que un elemento puede ser capaz de reaccionar con un número entero de átomos de hidrógeno o bien ser sustituido por un número entero de átomos de hidrógeno. En cualquier caso ese número entero es el que determina su capacidad de combinación y es lo que se conoce como ‘valencia’ de los elementos.
Pongamos un ejemplo para entenderlo mejor: de la fórmula del agua, H2O se deduce que el oxígeno actúa con una valencia 2 mientras que de la fórmula del metano, CH4, se deduce que el carbono interviene con valencia 4. Conviene recordar en este punto que no todos los elementos presentan una única valencia, los hay que tienen la posibilidad de emplear varias.
El concepto de valencia está relacionado con la configuración electrónica externa (o ‘electrones de valencia’) de los elementos y con la posición que ocupan en la tabla periódica. Así, los elementos del grupo I (metales alcalinos) tienen valencia 1, los del grupo II (metales alcalinotérreos) tienen valencia 2, etc.
Contenido relacionado
 ¿Cuántos elementos químicos hay?
¿Cuántos elementos químicos hay?
La Unión internacional de Química pura y aplicada (IUPAC) admitió oficialmente a comienzos de 2016 la existencia de 118 […]
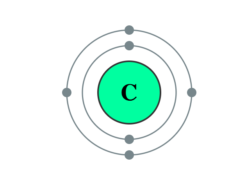 ¿Por qué el carbono da tantos compuestos distintos?
¿Por qué el carbono da tantos compuestos distintos?
El carbono da multitud de compuestos diferentes porque sus átomos tienen la capacidad de unirse tanto entre sí como con […]
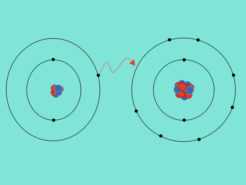 ¿Cómo se forman los enlaces químicos?
¿Cómo se forman los enlaces químicos?
Los enlaces químicos se forman ganando, cediendo o compartiendo electrones para alcanzar configuraciones electrónicas estables como por ejemplo […]



